International Journal of Molecular Sciences丨乳酸菌遗传转化进展:突破屏障与优化质粒工具

原创:微谨生物
发表期刊:International Journal of Molecular Sciences
发表年份:2025
文章题目:Advances in Genetic Transformation of Lactic Acid Bacteria: Overcoming Barriers and Enhancing Plasmid Tools
通讯作者:Aleksei S. Rozanov、Leonid A. Shaposhnikov(俄罗斯天狼星科技大学)
原文链接:DOI 10.3390/ijms26189146
乳酸菌(LAB)在食品发酵、益生菌递送和合成生物学中具有重要应用,但其遗传操作面临两大核心障碍:厚肽聚糖层形成的物理屏障,以及限制修饰(R-M)系统对未甲基化外源DNA的切割。许多菌株还对溶菌酶等细胞壁水解酶高度耐受,进一步增加了DNA导入难度。实践中,使用来自Dam⁻/Dcm⁻大肠杆菌的未甲基化质粒DNA,可有效规避R-M系统识别,使转化效率提升三个数量级以上。
1. 自然转化
自然转化是细菌主动摄取外源DNA的过程,需要细胞进入感受态。在LAB中,仅少数菌株存在天然感受态,如嗜热链球菌和部分乳酸乳球菌。通过添加合成感受态刺激肽和过表达ComX调控因子,可诱导这些菌株进入感受态,实现高达15 kb DNA片段的基因组整合。该方法可实现无标记编辑,但菌株依赖性极强,大多数LAB仍需人工转化。
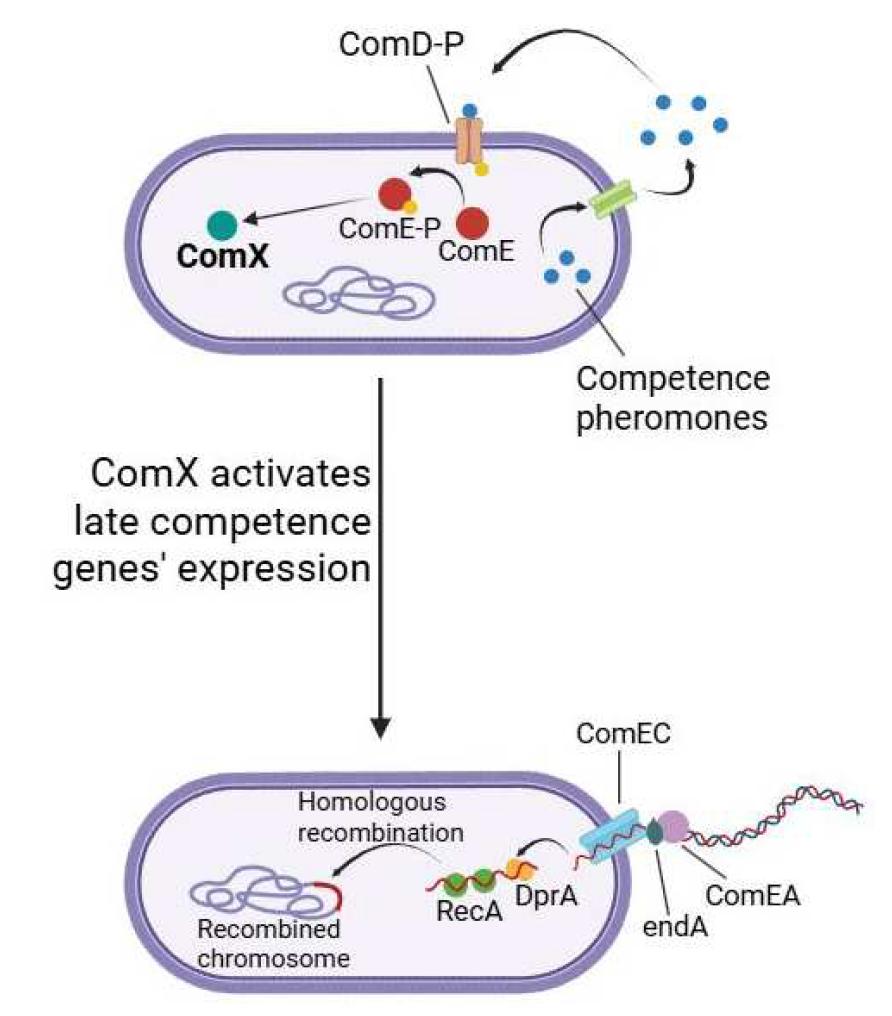
图1. 革兰氏阳性菌肺炎链球菌的自然转化机制
感受态信息素(群体感应肽)分泌到胞外,浓度达阈值后与跨膜复合物ComD结合,触发磷酸化级联反应,激活ComX表达。ComX作为替代σ因子,启动晚期感受态基因表达,包括DNA摄取装置和重组系统,使细胞进入感受态,外源DNA被RecA/DprA包被后进行同源重组。
2. 电穿孔
电穿孔是LAB中最广泛使用的人工转化方法。短电脉冲在细胞膜上形成瞬时孔道,使DNA进入。优化关键因素包括:
a. 细胞壁弱化剂:
- 甘氨酸:替代肽聚糖中的丙氨酸,抑制交联。6-8%甘氨酸可使植物乳杆菌转化效率提高30-100倍。
- 氯化钠:0.9 M NaCl诱导渗透胁迫,削弱细胞壁,使干酪乳杆菌效率达10⁵ CFU/μg DNA。
- 溶菌酶:水解肽聚糖,预处理可使效率提高30-1000倍。
- 青霉素:抑制肽聚糖交联,效率提高480倍。
- DL-苏氨酸:20-40 mM处理,使部分菌株获得转化能力。
b. 电脉冲参数:场强通常为12.5-15 kV/cm,电阻200-400 Ω,需针对菌株和生长阶段优化。
c. 恢复条件:使用含0.5 M蔗糖的恢复培养基,2-3小时恢复培养是关键。
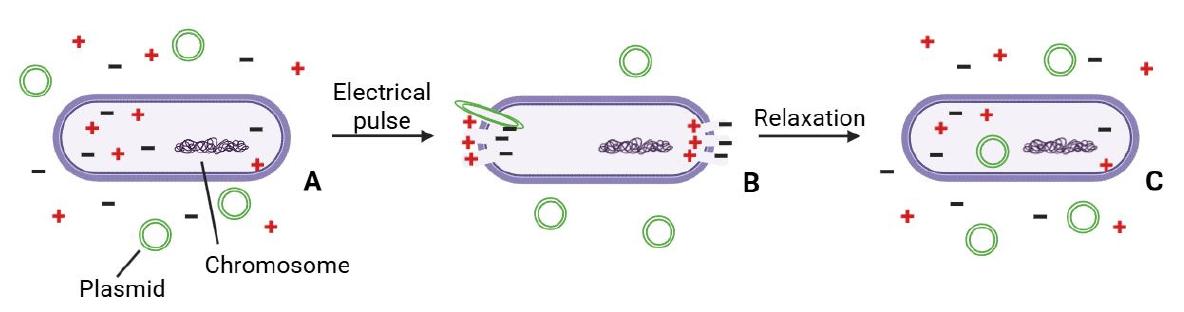
图2. 电穿孔原理示意图
(A)向细胞悬液中加入质粒;(B)施加电脉冲,细胞壁形成瞬时孔道,质粒进入细胞;(C)移除电脉冲,孔道闭合,部分细胞获得质粒并在恢复培养后形成转化子。
3. 接合转移
接合通过细胞接触直接转移DNA,可绕过R-M屏障并转移大片段。常用滤膜杂交法或平板杂交法,供体-受体比例约1:1,杂交时间6-24小时。使用携带RP4转移系统的大肠杆菌S17-1作为供体,可将质粒高效转移至干酪乳杆菌,效率达1.8×10⁻³/供体。近期开发的XPORT诱导型接合系统,通过调控必需转移基因表达,实现可控的水平基因转移。
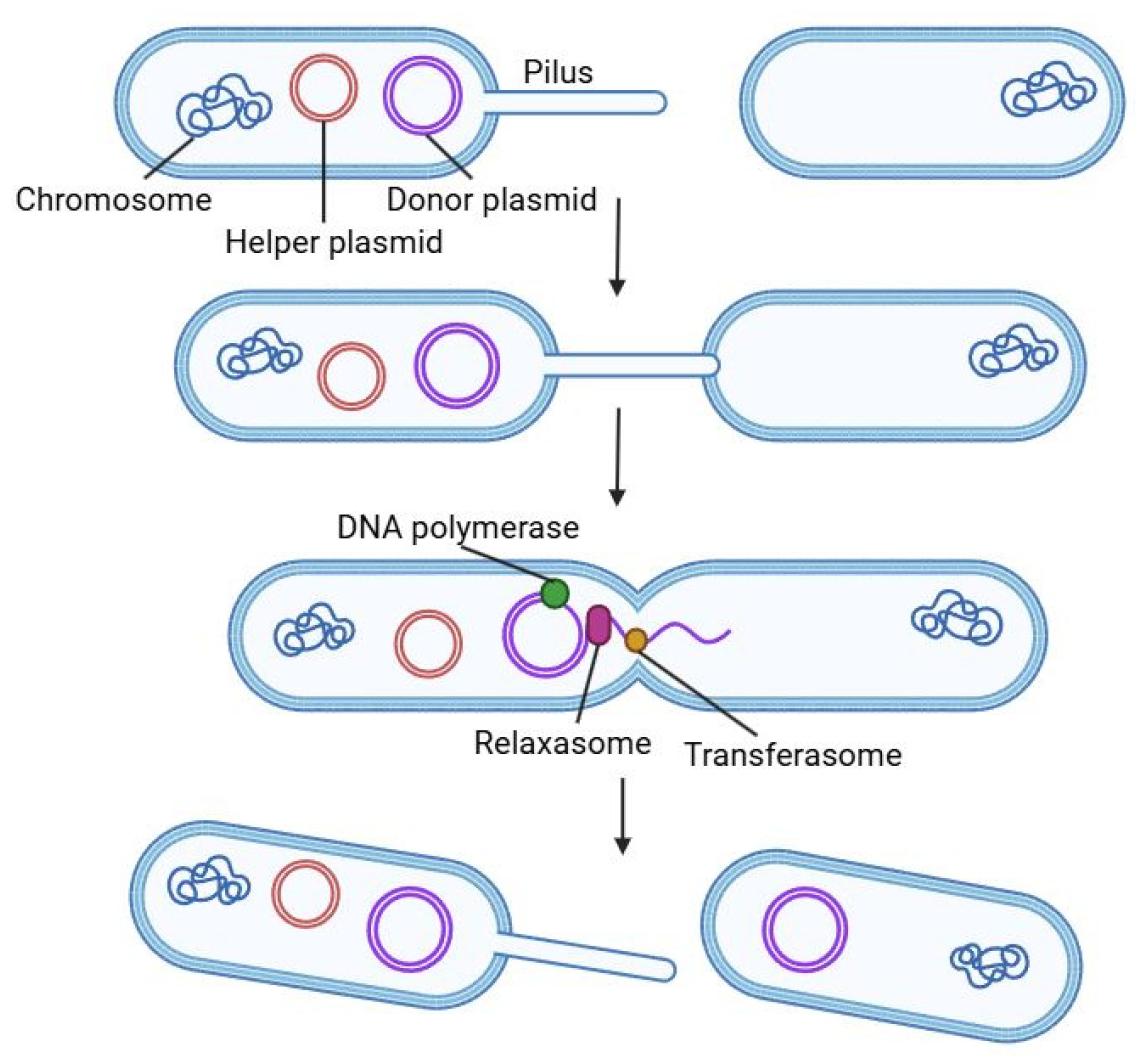
图3. 细菌接合转移示意图
供体细胞通过IV型分泌系统和接合菌毛与受体细胞连接,辅助质粒表达转移蛋白,供体质粒启动复制并立即通过松弛体-转移体装置进入受体细胞。
4. 噬菌体转导
噬菌体通过错误包装宿主DNA实现基因转移。在乳酸乳球菌、德氏乳杆菌和加氏乳杆菌中均有成功报道。LL-H噬菌体+pX3质粒系统在德氏乳杆菌中效率惊人,高达0.1-1转导颗粒/PFU,几乎全部噬菌体颗粒携带质粒DNA。加氏乳杆菌Φadh噬菌体系统也可高效递送质粒。但宿主范围窄是主要限制。
5. 基因枪
DNA包被的微粒(金、钨或纳米金刚石)经高压加速射入细胞,纯物理方法可突破顽固屏障。近期成功应用于长期难以转化的酒球菌。但设备昂贵、效率较低,仅作为最后手段。
表1. DNA导入方法比较
| 方法 | 典型效率 | 主要优点 | 主要缺点 | 最佳应用场景 |
|---|---|---|---|---|
| 自然转化 | 菌株依赖 | 无标记、基因组编辑 | 宿主范围极窄 | 嗜热链球菌等可诱导菌株 |
| 电穿孔 | 10⁴-10⁶ CFU/μg | 快速、通用、可优化 | 菌株差异大、R-M敏感 | 常规质粒转化、多数实验室菌株< |
| 接合 | 10⁻³-10⁻⁶/供体 | 可转移大片段、绕过R-M | 需供体-受体匹配 | 顽固菌株、工业菌改良 |
| 转导 | 菌株依赖 | 自然过程、效率可极高 | 宿主范围窄、需特定噬菌体 | 有合适噬菌体系统时 |
| 基因枪 | 较低 | 物理穿透、不依赖生物学 | 设备昂贵、细胞死亡率高 | 其他方法均失败的顽固菌株 |
1. 天然质粒与复制方式
LAB天然质粒主要采用两种复制方式:
a. 滚环复制(RCR):拷贝数高,但结构不稳定性,适合<10 kb插入片段
b. θ复制:拷贝数低,稳定性高,可容纳大片段
2. 穿梭载体
同时带有LAB复制子和大肠杆菌复制子,便于克隆操作。常用复制子包括pWV01(RCR型,广宿主)、pAMβ1(θ型)等。代表载体:pLES003(基于短乳杆菌pLB925A03)、pGYC4α(基于清酒乳杆菌pYC2)、pSIP系列(基于清酒乳杆菌质粒,诱导型表达)。
3. 食品级筛选标记
避免使用抗生素抗性基因,采用:
a. 营养缺陷互补:如alr(丙氨酸消旋酶)基因。
b. 细菌素免疫:如nisI(乳酸链球菌素免疫)、lcn972(乳球菌素972免疫)。
c. 代谢标记:如oroP(乳清酸转运蛋白)。
4. 整合载体与温敏型质粒
自杀质粒:如pORI19,携带LAB复制子但缺失repA基因,需辅助质粒pVE6007提供RepA。通过温度切换控制整合。
温敏型质粒:如pG⁺host9,基于pWV01的温敏突变体。在30℃允许温度下复制,37-39℃非允许温度下强制整合染色体,广泛用于基因敲除和敲入,最终可获得无外源标记的食品级工程菌。
5. 多质粒共存的策略
不同复制子分属不同不相容群。使用pWV01来源与pAMβ1来源的质粒可在同一菌株中共存。当前已有针对不同复制子分类的系统研究,指导多基因表达系统的构建。
乳酸菌遗传操作已取得显著进展,研究人员可根据菌株特性选择合适方法:电穿孔适用最广,接合和转导可攻克顽固菌株,自然转化实现无标记编辑,基因枪作为最后手段。
未来优先方向包括针对不同菌株建立模块化优化流程;绘制菌株甲基化修饰图谱,指导DNA甲基化工程;开发更多广宿主、稳定遗传的复制子;将食品级载体与CRISPR等平台结合,实现高效无痕改造,这些进展将直接推动食品级工程菌和益生菌活体生物药的开发应用。
主要参考文献:
[1] Spath, K.; Heinl, S.; Grabherr, R. Direct cloning in Lactobacillus plantarum: Electroporation with non-methylated plasmid DNA enhances transformation efficiency and makes shuttle vectors obsolete. Microb. Cell Fact. 2012, 11, 141.
[2] Welker, D.L.; Hughes, J.E.; Steele, J.L.; Broadbent, J.R. High efficiency electrotransformation of Lactobacillus casei. FEMS Microbiol. Lett. 2015, 362, 1–6.
[3] Palomino, M.M.; Allievi, M.C.; Prado-Acosta, M.; Sanchez-Rivas, C.; Ruzal, S.M. New method for electroporation of Lactobacillus species grown in high salt. J. Microbiol. Methods 2010, 83, 164–167.
[4] Samperio, S.; Guzmán-Herrador, D.L.; May-Cuz, R.; Martín, M.C.; Álvarez, M.A.; Llosa, M. Conjugative DNA Transfer from E. coli to Transformation-Resistant Lactobacilli. Front. Microbiol. 2021, 12, 606629.
[5] Bron, P.A.; Marcelli, B.; Mulder, J.; van der Els, S.; Morawska, L.P.; Kuipers, O.P.; Kok, J.; Kleerebezem, M. Renaissance of traditional DNA transfer strategies for improvement of industrial lactic acid bacteria. Curr. Opin. Biotechnol. 2019, 56, 61–68.
[6] Damelin, L.H.; Mavri-Damelin, D.; Klaenhammer, T.R.; Tiemessen, C.T. Plasmid Transduction Using Bacteriophage Φadh for Expression of CC Chemokines by Lactobacillus gasseri ADH. Appl. Environ. Microbiol. 2010, 76, 3878–3885.
[7] Chen, M.; Chen, Q. Gene manipulation in Oenococcus oeni based on a newly applicable gene gun technology. Front. Microbiol. 2025, 16, 1545266.
[8] Nguyen, T.-T.; Mathiesen, G.; Fredriksen, L.; Kittl, R.; Nguyen, T.-H.; Eijsink, V.G.H.; Haltrich, D.; Peterbauer, C.K. A Food-Grade System for Inducible Gene Expression in Lactobacillus plantarum Using an Alanine Racemase-Encoding Selection Marker. J. Agric. Food Chem. 2011, 59, 5617–5624.
